「国際共同治験(グローバル試験)は普通の治験と何が違うのでしょうか?」の質問と回答のページです。質問に対しての回答投稿が可能です。マナーを守って有意義に利用しましょう。(削除申請はこちらからお願いします)
国際共同治験(グローバル試験)は普通の治験と何が違うのでしょうか?
 質問
質問

国際共同治験(グローバル試験)は普通の治験と何が違うのでしょうか?
未経験からCRA(臨床開発モニター)への転職を検討しているものです。ネット上でよく国際共同治験(グローバル試験)という記述を目にするのですが、普通の治験と何が違うのでしょうか。やはり大変だったりするのでしょうか。詳しい人がいらっしゃいましたら教えて下さい。 2016年8月16日
2016年8月16日  27571
27571
 AIによる要約
AIによる要約
 マンガでわかる
マンガでわかる

 イラスト・図解でわかる
イラスト・図解でわかる
 みんなの回答一覧
みんなの回答一覧
- 複数の国で統一したプロトコルに基づいて実施する試験 ベストアンサー
-
国際共同治験とは、簡単に言うと「複数の国で統一したプロトコル(治験実施計画書)に基づいて実施する試験」と言えます。
昨今、国際共同治験が盛んである背景としては、ドラッグラグ(いわゆる承認済医薬品の地域間格差)の解消や、1カ国では症例集積が難しい疾患での医薬品開発が多くなってきていることが挙げられます。
統一したプロトコルですから、基本言語は英語で、各種資料や会議を含めて圧倒的に英語を使用する機会が多いでしょう。
FDA(アメリカ), EMA(ヨーロッパ), PMDA(日本)と各国の規制当局間では、データの解釈や申請要件に若干の違いがあり、その点の調整が必要だったりします。
通常の治験は、日本での承認を取得するために計画されていますので、日本の実情にあった運用になっていますが、国際共同治験の場合はそう簡単ではありません。
また臨床現場では、併用禁止薬に違いがあったり、臨床検査の検体を海外ラボに送る必要があったりと、様々な細かな対応事項があります。
大変ですが、今後、増え続けるであろう国際共同治験のニーズを考えると、国際共同治験の経験は有用だと思います。
 2016年9月5日
2016年9月5日
役に立った(8)
- 英語力が必要になる点が違います。 ベターアンサー
-
現在は各製薬企業も国際共同治験の経験を積んでおり、以前のように何をすれば良いか分からないということはなくなっています。
国際共同治験(グローバル試験)と普通の治験の主な違いは、グローバル特有の書類の書き方や試験の進め方を覚える必要があることです。現在は各社にノウハウが蓄積されていますので、書類の書き方や試験の進め方が分からないということは少ないと思います。
ただし、ノウハウが蓄積されているとはいえ、提出書類は英語で作成する必要がありますので、読んだり書いたりできる最低限の英語力は必要になります。どこの会社も翻訳ツールが充実していたり、翻訳の部署が設けられていたりしますので、一般社員のうちは自己学習でなんとかなる場合が多いです。
リーダー以上になると試験について海外との打ち合わせが必要になるため、読み書きだけでなく、電話会議で英語を使用して交渉できる英語力が必要となります。試験の進捗を正確に伝えたり、要求に同意してもらう英語力が必要になるため、ビジネスレベルでの英語力が必要になると言えます。
また、海外とは時差があるため、深夜に何通ものメールが届いたり、早朝や深夜に電話会議があったりするため、国内の治験よりも体力が求められると言えます。とはいえ、よほどの緊急でないかぎり、深夜に業務の対応が必要になることはありませんので、慣れてしまえば割り切れると思います。
 2016年8月16日
2016年8月16日
役に立った(2)
- 国際共同治験(グローバルスタディ)の歴史 ベターアンサー
-
従来は海外で過去に行われた治験データを、日本国内の治験データに追加・代用するブリッジングスタディによって臨床開発が行われていましたが、現在はより早く治験を行い、結果を分析することができる国際共同治験(グローバルスタディ)が主流となっています。
国際共同治験(グローバルスタディ)のメリットとして
・新薬の世界同時開発・申請・承認が可能である。
・ドラッグ・ラグを解消できる
・複数の国や地域で被験者を集めるため、必要な人数を短期間で集められる。
・集まる症例数が多く、副作用を見つけやすい。発現頻度が低い副作用を見つけられる可能性も高まる。
・薬の有効性・安全性に民族差があるかどうかを把握しやすい。
などがあげられます。
これにより製薬会社は新薬の上市時期を早めて売上を最大化することが可能になります。
 2016年8月16日
2016年8月16日
役に立った(2)
- 臨床開発用語集より 公式
-
https://cra-bank.com/chikenyougosyuu#d7
グローバル治験(グローバルスタディ/グローバル試験)とは
https://cra-bank.com/chikenyougosyuu#b43
ローカル治験(ローカルスタディ/国内治験)とは
 2024年5月28日
2024年5月28日
- グローバル試験のしんどい点について
-
グローバル治験とローカル治験を比べた場合、英語を使う頻度が増えることや、チームの意思疎通の難易度が上がる点が異なります。
海外の担当者とのメールのやりとりは英語になりますし、英語のみで行われるWEB会議に参加したりする場合も稀にあります。時差のためメールの返信が遅れるだけでなく、ミーティングが行われる時間は夜遅くや早朝になることがきほんです。
英語のメールでのやりとりは別に問題ありませんが、深夜3時に何通もメールが届くと寝不足になりますし、英語での打ち合わせは意思疎通するだけで精一杯です。グローバルなチームで働く面白さはありますが、しんどいと思うことの方が多いですね。
ICH-GCPなどの規制の違いについては、弊社は専門のチームがあるため、わからない点はすぐに教えてもらえたため問題なく対応できました。
 2024年3月27日
2024年3月27日
役に立った(0)
- 国際共同治験と普通の治験の違い AI
-
国際共同治験(グローバル試験)とは
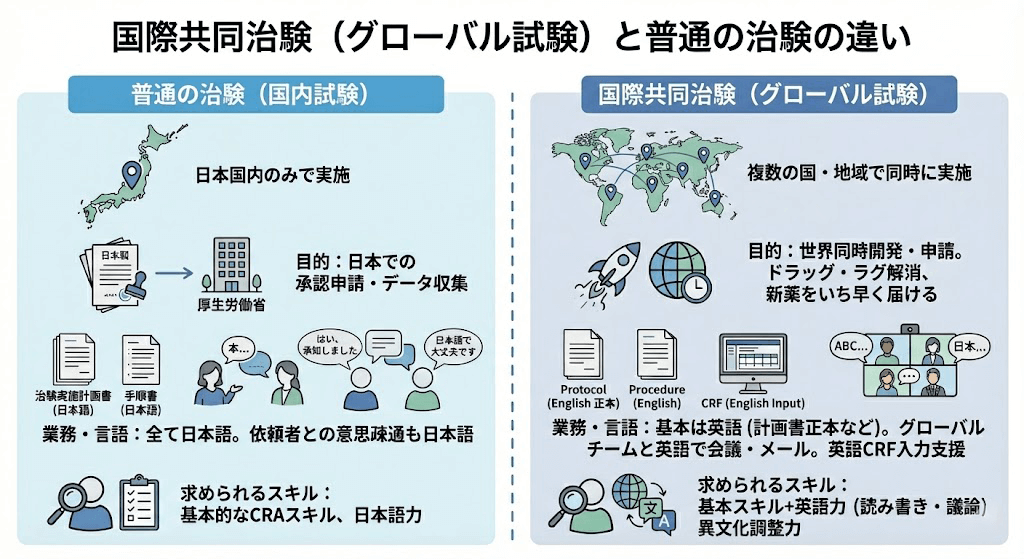
国際共同治験(グローバル試験)とは、複数の国や地域で同時に行われる治験のことです。これは、新薬を世界中で迅速に使えるようにするために行われます。一方、通常の治験は、基本的に単一の国または地域内で行われます。
国際共同治験と通常の治験の主な違い
国際共同治験と通常の治験には、以下のような違いがあります。
◆ 実施地域: 国際共同治験は複数の国や地域で実施されますが、通常の治験は単一の国または地域で実施されます。
◆ 目的: 国際共同治験は新薬のグローバル展開を目的とすることが多いですが、通常の治験は国内での承認取得を主な目的とします。
◆ 規制要件: 国際共同治験は複数の国の規制要件に従う必要がありますが、通常の治験は国内の規制要件に従います。
◆ コミュニケーション: 国際共同治験では、異なる言語や文化を持つ関係者とのコミュニケーションが必要となります。
◆ 資料: 治験実施計画書(プロトコル)、症例報告書(CRF)などの資料は、多くの場合英語で作成され、複数の言語に翻訳されることがあります。
◆ モニタリング: 国際共同治験では、複数の国や地域の治験実施施設をモニタリングする必要があるため、出張の機会が多くなる可能性があります。
国際共同治験の大変な点
国際共同治験は、通常の治験に比べて以下のような点で大変と言われています。
◆ 多言語・多文化対応: 異なる言語や文化を持つ関係者とのコミュニケーションは、誤解やコミュニケーション不足につながる可能性があります。
◆ 各国の規制対応: 各国の規制要件を理解し、遵守する必要があります。規制の違いにより、治験の手順や資料作成に違いが生じる場合があります。
◆ 時差: 異なるタイムゾーンで働く関係者との連携が必要となるため、時間調整が難しい場合があります。
◆ 出張: 複数の国や地域への出張が必要となるため、体力的な負担や生活リズムの調整が必要となります。
◆ 資料の翻訳・管理: 多くの資料が複数の言語で作成されるため、翻訳や資料管理が煩雑になる場合があります。
国際共同治験のメリット
大変な点もありますが、国際共同治験には以下のようなメリットもあります。
◆ 早期のグローバル展開: 新薬を世界中で迅速に使えるようにすることで、患者さんにいち早く新しい治療を提供できます。
◆ 多様なデータ収集: 異なる人種や民族のデータを含めた多様なデータを収集することで、薬の有効性や安全性をより正確に評価できます。
◆ 開発コストの削減: 複数の国で同時に治験を行うことで、開発期間を短縮し、開発コストを削減できる場合があります。
CRAとして国際共同治験に関わる場合
CRAとして国際共同治験に関わる場合は、通常の治験に加えて、以下のようなスキルや経験が求められることが多いです。
◆ 高い英語力: 海外の関係者とのコミュニケーションや英語資料の読解・作成に必要です。
◆ 異文化理解: 異なる文化を持つ関係者との円滑なコミュニケーションを図るための理解力や柔軟性が求められます。
◆ グローバルな視点: 世界的な視点を持って治験全体を俯瞰し、各国の規制要件や文化の違いを考慮したモニタリングを行う必要があります。
◆ コミュニケーション能力: 関係者間の調整や情報伝達を円滑に行うための高いコミュニケーション能力が求められます。
◆ 出張への対応力: 海外出張に抵抗がなく、柔軟に対応できることが求められます。
まとめ
国際共同治験は、通常の治験に比べて複雑で大変な面もありますが、グローバルな医薬品開発に貢献できるという大きな魅力があります。CRAとしてステップアップを目指す上で、国際共同治験に関わる経験は非常に貴重なものとなるでしょう。未経験からCRAを目指す場合でも、英語力や異文化理解を意識することで、将来的に国際共同治験で活躍できる可能性が広がります。
項目 通常の治験(国内試験) 国際共同治験(グローバル試験) 実施国 日本国内のみ 複数国で同時またはほぼ同時に実施 目的 日本国内での医薬品の承認取得 複数国での同時承認取得、早期の世界展開 対象患者 日本人患者 多様な人種・民族の患者 治験実施計画書(プロトコル) 日本の規制・文化に合わせて作成 複数国の規制・文化を考慮して作成(共通プロトコルが基本) 言語 基本的に日本語 英語が主要言語となることが多い(文書、コミュニケーション) 規制当局 日本の規制当局(PMDA) 各国の規制当局 CRAの業務 日本語でのコミュニケーション、国内の規制に準拠した業務 英語でのコミュニケーション、複数国の規制に準拠した業務、海外担当者との連携 大変さ(CRA視点) ◆ 国内の規制に集中して対応できる。
◆ コミュニケーションは日本語が中心。◆ 複数国の規制に対応する必要があるため、より多くの知識が求められる。
◆ 英語でのコミュニケーションが必須となるため、高い英語力が必要。
◆ 時差や文化の違いを考慮した対応が必要。
◆ 緊急時の対応が複雑になる場合がある。メリット(CRA視点) ◆ 国内の治験経験を確実に積める。
◆ 言語の壁が少ないため、業務に集中しやすい。◆ グローバルな視点や経験を得られる。
◆ 高度な英語力を身につけられる。
◆ キャリアアップの機会が広がる可能性がある。
◆ 多様な文化に触れることができる。
※CRA転職に特化したAIアシスタントを利用したい方はこちらから

















 年収査定はこちら
年収査定はこちら
 合格予想はこちら
合格予想はこちら
 掲示板で質問をする
掲示板で質問をする






 CRA
CRA

 CRAの
CRAの
 CRAの
CRAの
 CRAの
CRAの
 CRAの
CRAの
 CRAに
CRAに
 CRAの
CRAの
 CRO
CRO
 CRO
CRO
 臨床開発
臨床開発
 製薬会社と
製薬会社と
 CROから
CROから



 2027年4月からの転職
2027年4月からの転職 CRA未経験特集
CRA未経験特集 薬剤師特集
薬剤師特集 MR特集
MR特集 看護師特集
看護師特集 臨床検査技師特集
臨床検査技師特集 保健師特集
保健師特集 獣医師特集
獣医師特集 理系大卒・院卒特集
理系大卒・院卒特集 CRC経験者特集
CRC経験者特集


 求人検索
求人検索  ログイン
ログイン 会員さま専用
会員さま専用 CRAの仕事
CRAの仕事  臨床開発業界の研究
臨床開発業界の研究 経験・資格別の注意点
経験・資格別の注意点 応募書類の作成
応募書類の作成 面接・適性検査の対策
面接・適性検査の対策 みんなのクチコミ
みんなのクチコミ みんなの質問と回答
みんなの質問と回答 転職成功事例
転職成功事例 マンガで分かるCRA
マンガで分かるCRA 便利な機能
便利な機能 相談/年収査定/合格予想
相談/年収査定/合格予想 2027年から働くには?
2027年から働くには? 退職手続き
退職手続き 開催中のキャンペーン
開催中のキャンペーン 《CRAばんく》とは
《CRAばんく》とは