「症例SDV、必須文書閲覧数の事前準備について教えてください」の質問と回答のページです。質問に対しての回答投稿が可能です。マナーを守って有意義に利用しましょう。(削除申請はこちらからお願いします)
症例SDV、必須文書閲覧数の事前準備について教えてください
 質問
質問

症例SDV、必須文書閲覧数の事前準備について教えてください
来週初めてSDVをします。
事前準備が大切だと言われましたが、何を準備したらいいのか分かりません。
情報、ツール、確認事項などを教えて頂きたいです。 2023年5月26日
2023年5月26日  4386
4386
 AIによる要約
AIによる要約
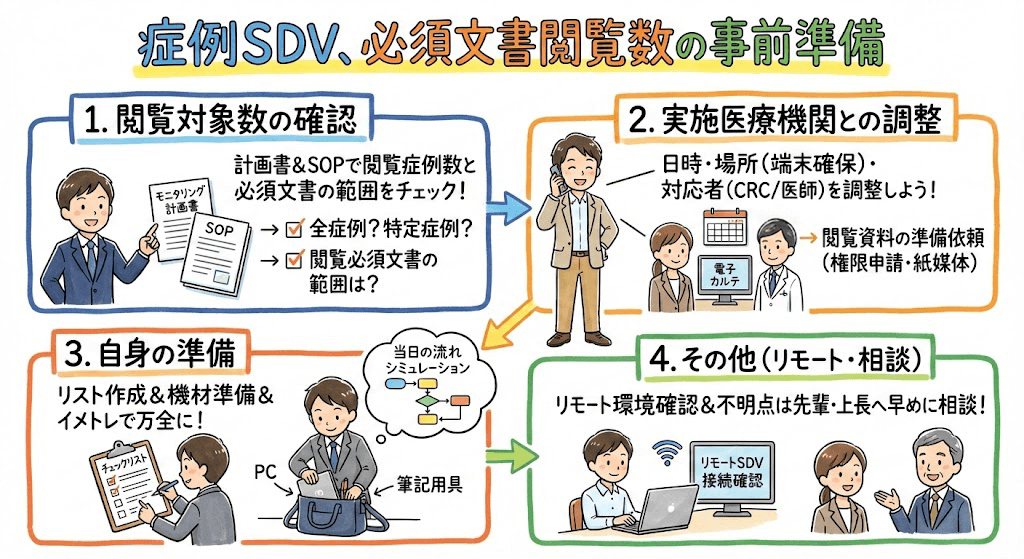
1) SDVの準備は、治験概要の把握、関連資料の準備、確認項目の整理、医療機関への連絡が重要。
2) SDV当日のスケジュール管理が大切。余裕を持った計画と必須文書の把握がポイント。
3) SDV業務の基本的な流れを掴むことが重要。事前準備は治験概要、関連資料、確認項目、医療機関連絡。
4) 初めてのSDVでは不明点を質問、時間配分を意識、記録を残し、医療機関とのコミュニケーションを重視。
 マンガでわかる
マンガでわかる

 イラスト・図解でわかる
イラスト・図解でわかる
 みんなの回答一覧
みんなの回答一覧
- 初めてのSDVを成功させるための準備のコツ ベターアンサー
-
MRからCRAに転職して初めてSDVを行った時は緊張しましたが、入念な事前準備をしたことでスムーズに進められました。
まずは、SDVを行う症例の組入基準や前回のモニタリング記録をしっかり確認することが大切だと思います。電子カルテの閲覧申請やIDの発行手続きも早めに済ませておきましょう。
SDVで重要なのは、症例報告書とカルテの照合ポイントを明確にしておくことです。私は治験実施計画書を読み返し、重要な観察項目をリストアップしました。
SDV当日のスケジュール管理も大切です。私の場合、直前確認でペースが遅れてしまい、予定の半分も終わらないこともありりました。その経験から、1症例あたり2時間程度の余裕を持って計画を立てています。また必須文書の種類と保管場所も事前に把握しておくと、当日スムーズに進むと思います。
SDV業務は基本的な流れを掴めば、それほど難しくないと考えます。
 2024年11月13日
2024年11月13日
役に立った(2)
- 治験薬のSDVについて
-
上司や先輩に確認することをお勧めしますが、治験薬のSDVについて基本的な確認事項を説明させていただきます。
1. 治験薬の搬入時における温度管理について、逸脱が発生していないかを確認します。
2. 搬入された治験薬については、その全数が治験薬管理表に正確に記載されているかを確認します。
3. 被験者への治験薬払い出しに関して、以下の2点を確認します。
・IVRSで指示された払い出し内容と実際の払い出しが一致していること
・治験薬管理表に払い出しの記録が正確に記載されていること
4. 被験者からの治験薬返却について、以下の事項を確認します。
・返却された治験薬が治験薬管理表に正確に記録されていること
・返却数および錠数の記録が正確であること
・服用率の計算が適切に行われていること
5. 治験薬の廃棄または施設からデポへの返却に関して、それらの記録が治験薬管理表に漏れなく記載されていることを確認します。
6. 治験薬管理表における記載者(処方や返却等の記録者)について、その署名が担当者のものであることを確認します。
7. 施設での治験薬保管状況について、保管期間中の温度逸脱が発生していないかを確認します。
8. 必要書類に関して、以下の2点を確認します。
・保管すべき資料が適切に保管されていること
・必要な署名が漏れなく記載されていること
 2023年12月22日
2023年12月22日
役に立った(0)
- SDVの事前準備について AI
-
SDVの事前準備は、治験概要の把握、関連資料の準備、確認項目の整理、医療機関への連絡の4つの段階に分けられます。これらの準備をしっかりと行うことで、当日のSDVをスムーズに進めることができます。
以下に、それぞれの段階で準備すべき情報、ツール、確認事項などを詳しく説明します。
1. 治験概要の把握
まず、SDVを行う治験について、以下の点を十分に理解しておく必要があります。
◆ 治験実施計画書(プロトコル): 治験の目的、デザイン、評価項目、選択基準・除外基準、スケジュールなど、治験の全体像を把握するために、プロトコルを熟読しましょう。特に、SDVで確認するデータ項目がどの部分に記載されているかを確認しておくと、当日の作業がスムーズになります。
◆ 症例報告書(CRF): CRFの構成、記載方法、記入上の注意点などを確認しましょう。特に、SDVで照合するデータ項目がCRFのどの部分に記載されているかを確認しておくと、当日の作業がスムーズになります。
◆ モニタリング手順書: 治験依頼者(製薬会社)またはCRO(医薬品開発業務受託機関)が作成したモニタリング手順書を確認し、SDVの手順や方法、使用するツールなどを把握しましょう。
◆ 治験薬概要: 治験薬の作用機序、用法・用量、投与方法、禁忌、重要な副作用など、基本的な情報を把握しておきましょう。
◆ 関連する医学・薬学的知識: 治験対象疾患や関連する医学・薬学的知識を復習しておきましょう。
2. 関連資料の準備
SDVに必要な資料を事前に準備しておきましょう。
◆ 症例報告書(CRF): SDV対象症例のCRFを準備しましょう。電子CRFの場合は、アクセス権限などを確認しておきましょう。
◆ 原資料リスト: どの原資料(カルテ、検査データ、同意説明文書など)を照合するのかをリストアップしておきましょう。
◆ チェックリスト: SDVで確認する項目をリストアップしたチェックリストを作成しておくと、確認漏れを防ぐことができます。
◆ その他: 必要に応じて、同意説明文書、治験薬投与記録、検査データ、画像データなどを準備しましょう。
3. 確認項目の整理
SDVで具体的に何を確認するのかを整理しておきましょう。
◆ 選択基準・除外基準の適合性: 治験参加者が選択基準を満たし、除外基準に該当しないかを確認します。
◆ 同意取得の状況: 同意説明文書への署名日、説明者、同意取得状況などを確認します。
◆ CRF記載内容と原資料の整合性: CRFに記載されているデータが、原資料と一致しているかを確認します。特に、主要評価項目、安全性評価項目、重要な副次評価項目などは、重点的に確認しましょう。
◆ 有害事象の有無と内容: 有害事象が発生した場合、その内容、発現日、重篤度、処置などを確認します。
◆ 治験薬の投与状況: 治験薬の投与日、投与量、投与方法などを確認します。
◆必須文書の確認: 治験に関連する必須文書(例:治験審査委員会承認書、治験契約書、治験分担医師リストなど)が適切に保管されているかを確認します。
4. 医療機関への連絡
SDVの日程調整や必要な準備について、事前に医療機関に連絡しておきましょう。
◆ SDVの日程調整: 医療機関の担当者(CRCなど)と連絡を取り、SDVの日程を調整しましょう。
◆ 必要な資料の準備依頼: 医療機関に、SDVに必要な資料(カルテなど)の準備を依頼しましょう。
◆ 質問事項の確認: 医療機関に、SDVに関して質問事項があれば事前に伝えておきましょう。
◆ 訪問場所とアクセス方法の確認: 医療機関の場所、訪問場所、アクセス方法などを確認しておきましょう。
初めてのSDVで特に注意すべきこと
◆ 不明点は遠慮せずに質問する: わからないことや不安なことがあれば、先輩CRAや上司に遠慮せずに質問しましょう。
◆ 時間配分を意識する: 事前にSDVにかかる時間を見積もり、時間配分を意識して作業を進めましょう。
◆ 記録をしっかりと残す: SDVで確認した内容や疑問点などを、記録として残しておきましょう。
◆ 医療機関とのコミュニケーションを大切にする: 医療機関の担当者とは、丁寧なコミュニケーションを心がけましょう。
これらの準備をしっかりと行うことで、初めてのSDVをスムーズに進めることができるはずです。落ち着いて、一つ一つ丁寧に確認していきましょう。
事前準備 具体的な内容 理由 確認事項/ツール 治験概要の確認 ◆ 治験の目的、デザイン、評価項目などを改めて確認する。
◆ 特に、SDVで重点的に確認すべき項目(主要評価項目、安全性情報など)を把握する。SDVの目的は、治験がプロトコル(治験実施計画書)に従って適切に行われているかを確認することであるため、治験概要の理解は必須。 ◆ プロトコル(治験実施計画書)
◆ 治験薬概要書
◆ モニタリング手順書SDV対象症例の確認 ◆ SDV対象となる症例(全症例か、一部症例か、など)を確認する。
◆ 症例リストを入手し、症例番号や登録日などを把握する。SDVの対象を明確にすることで、効率的に作業を進めることができる。 ◆ 症例リスト 原資料の特定 ◆ どの資料が原資料となるか(カルテ、検査データ、同意書など)を特定する。
◆ 電子カルテの場合は、アクセス方法や操作手順を確認する。原資料を特定することで、SDV当日にスムーズに閲覧できる。 ◆ モニタリング手順書
◆ 医療機関の担当者への確認症例報告書(CRF)の確認 ◆ 確認対象のCRFを入手し、記載内容を事前に確認する。
◆ CRFの記載方法や記入ルールなどを確認する。CRFの内容を事前に把握することで、SDV当日に効率的に照合作業を進めることができる。 ◆ CRF(症例報告書)
◆ CRF記入マニュアル医療機関との連絡 ◆ SDVの日程、時間、場所などを医療機関の担当者と調整する。
◆ SDVに必要な資料や準備について、医療機関に事前に依頼する。スムーズなSDV実施のため、医療機関との連携は不可欠。 ◆ 医療機関の担当者への連絡(電話、メールなど) SDVに必要なツールの準備 ◆ SDVチェックリスト、筆記用具、電卓、必要に応じて電子機器(ノートPC、タブレットなど)を準備する。
◆ 電子カルテにアクセスする場合は、必要なID、パスワードなどを確認する。効率的なSDV実施のため、必要なツールを事前に準備しておく。 ◆ SDVチェックリスト
◆ 筆記用具
◆ 電卓
◆ ノートPC、タブレットなど
◆ 電子カルテのID、パスワードGCP/関連法規制の確認 ◆ GCP(医薬品の臨床試験の実施の基準に関する省令)や関連法規制(例:個人情報保護法)など、SDVに関わる法令を改めて確認する。 法令遵守はSDVの基本。 ◆ GCP省令
◆ 関連法規制その他 ◆ 移動手段や宿泊先などを手配する(出張の場合)。
◆ 当日の服装や持ち物などを確認する。スムーズなSDV実施のため、その他の準備も怠らない。 ◆ 出張手配
◆ 持ち物リスト
※CRA転職に特化したAIアシスタントを利用したい方はこちらから















 年収査定はこちら
年収査定はこちら
 合格予想はこちら
合格予想はこちら
 掲示板で質問をする
掲示板で質問をする






 CRA
CRA

 CRAの
CRAの
 CRAの
CRAの
 CRAの
CRAの
 CRAの
CRAの
 CRAに
CRAに
 CRAの
CRAの
 CRO
CRO
 CRO
CRO
 臨床開発
臨床開発
 製薬会社と
製薬会社と
 CROから
CROから



 2027年4月からの転職
2027年4月からの転職 CRA未経験特集
CRA未経験特集 薬剤師特集
薬剤師特集 MR特集
MR特集 看護師特集
看護師特集 臨床検査技師特集
臨床検査技師特集 保健師特集
保健師特集 獣医師特集
獣医師特集 理系大卒・院卒特集
理系大卒・院卒特集 CRC経験者特集
CRC経験者特集


 求人検索
求人検索  ログイン
ログイン 会員さま専用
会員さま専用 CRAの仕事
CRAの仕事  臨床開発業界の研究
臨床開発業界の研究 経験・資格別の注意点
経験・資格別の注意点 応募書類の作成
応募書類の作成 面接・適性検査の対策
面接・適性検査の対策 みんなのクチコミ
みんなのクチコミ みんなの質問と回答
みんなの質問と回答 転職成功事例
転職成功事例 マンガで分かるCRA
マンガで分かるCRA 便利な機能
便利な機能 相談/年収査定/合格予想
相談/年収査定/合格予想 2027年から働くには?
2027年から働くには? 退職手続き
退職手続き 開催中のキャンペーン
開催中のキャンペーン 《CRAばんく》とは
《CRAばんく》とは